康方生物/正大天晴抗PD-1單抗新適應癥申報上市
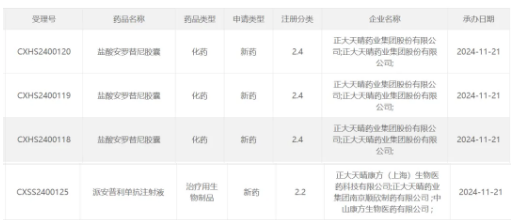
今日(11月21日),中國國家藥監(jiān)局藥品審評中心(CDE)官網公示�����,康方生物和正大天晴在研的抗PD-1抗體派安普利單抗注射液�,以及正大天晴在研的鹽酸安羅替尼膠囊上市申請獲得受理。
今年9月���,派安普利單抗聯(lián)合安羅替尼一線治療晚期肝細胞癌的3期研究結果在歐洲腫瘤內科學會(ESMO)年會公布���。正大天晴彼時新聞稿表示,將就該聯(lián)合療法的新適應癥向CDE遞交上市申請����。由此推測,本次獲受理的可能是一項聯(lián)合療法上市申請��,用于一線治療晚期肝細胞癌��。
截圖來源:CDE官網
派安普利單抗(penpulimab)是一款新型差異化抗PD-1單抗,該產品由康方生物研發(fā)�����,并由康方生物與正大天晴合資的正大天晴康方負責后續(xù)開發(fā)和商業(yè)化��。目前���,派安普利單抗已經在中國獲批3項適應癥,涵蓋非小細胞肺癌��、霍奇金淋巴瘤����、鼻咽癌。此外�����,該產品一線治療轉移性鼻咽癌的上市申請已提交�,治療肝癌、胃癌等適應癥的后期階段臨床研究也正在推進�。
安羅替尼(anlotinib)是正大天晴開發(fā)的新型小分子多靶點(VEGFR/PDGFR/FGFR/c-kit)酪氨酸激酶抑制劑(TKI),于2018年在中國首次獲批上市��,目前已經在中國獲批多個腫瘤適應癥。
在2024年ESMO年會上�,安羅替尼聯(lián)合派安普利單抗一線治療晚期肝細胞癌的3期臨床研究成果首次亮相。該研究取得了“雙終點陽性”:中位無進展生存期(PFS)為6.9個月�,中位總生存期(OS)為16.5個月,PFS和OS均達到預設終點�����。
具體而言����,這是一項隨機對照、開放��、3期研究(APOLLO研究)���,評估了鹽酸安羅替尼膠囊聯(lián)合派安普利單抗對比索拉非尼一線治療晚期肝細胞癌(HCC)�。APOLLO研究(ALTN-AK105-III-02)共納入晚期肝癌患者649例��,其中40.9%的受試者伴有大血管侵犯�、甲胎蛋白(AFP) ≥400 ng/mL的比例達到49.2%。研究結果顯示���,試驗組中位PFS為6.9個月�,對照組為2.8個月,疾病進展風險顯著降低了47%��。試驗組中位OS為16.5個月��,對照組為13.2個月���,死亡風險顯著降低了31%�����。安全性分析顯示�����,安羅替尼聯(lián)合派安普利單抗的安全性數據與已知風險相符,未出現新的安全性信號���。
據2022年全球癌癥數據統(tǒng)計��,原發(fā)性肝癌位居全球惡性腫瘤發(fā)病率第6位����,死亡率第3位�。原發(fā)性肝癌中75%-85%為肝細胞癌(HCC)���,由于HCC起病隱匿,早期癥狀不明顯��,多數患者確診時已處于晚期�����,失去根治性手術治療機會�。近年來,免疫治療的快速發(fā)展正在改變晚期肝癌的治療格局�,尤其是靶免聯(lián)合治療方案已成為晚期HCC的重要一線治療模式。
希望該聯(lián)合療法后續(xù)研究和上市進展順利��,早日為患者帶來新的治療選擇����。
聲明:本文版權歸原作者所有,轉載文章僅為傳播更多信息�,如作者信息標記有誤��,或侵犯您的版權����,請聯(lián)系我們�����,我們將在及時修改或刪除內容���,聯(lián)系郵箱:marketing@360worldcare.com