詹啟敏院士團隊:揭示食管鱗狀細胞癌相關惡病質的有前途靶點
2024年9月26日,中國醫(yī)學科學院���、北京協(xié)和醫(yī)學院詹啟敏院士團隊在期刊《Signal Transduction and Targeted Therapy》上發(fā)表了題為“GRP75 triggers white adipose tissue browning to promote cancer-associated cachexia”的研究論文���。研究結果揭示了腫瘤來源的GRP75在惡病質發(fā)展過程中���,調節(jié)白色脂肪組織褐變的新機制���,并提出了一種潛在的以白色脂肪組織為中心的早期惡病質干預靶向方法。
研究介紹
惡病質起源于希臘語“kakos”和“hexis”���,意思是“不良狀態(tài)”���,是癌癥患者的主要并發(fā)癥之一,是一種致命的消耗綜合征���,影響50-80%的癌癥患者���,消化系統(tǒng)腫瘤的患病率最高。在臨床實踐中���,惡病質被認為是一個連續(xù)體���,具有3個診斷階段:前惡病質、惡病質和難治性惡病質���。一旦患者達到難治期���,他們就會處于嚴重的身體衰退狀態(tài)���,其特征是侵襲性高分解代謝和對藥物反應不佳,這使得有效的減肥管理具有挑戰(zhàn)性���。
惡病質影響肌肉以外的多種組織���,包括白色脂肪組織 (WAT)。從初始診斷到復發(fā)���,計算機斷層掃描圖像上骨骼肌、皮下脂肪和內臟脂肪面積的減少程度與非小細胞肺癌復發(fā)后預后較差呈正相關���,表明身體成分在預后預測中的潛在效用���。此外,WAT丟失的程度與惡病質癌癥患者的生存和預后相關���。
在這項研究中���,通過設置3個時間點(T-1到T-3)���,團隊系統(tǒng)地描述了物理參數的動態(tài)變化,并在建立的食管鱗狀細胞癌(ESCC)誘導的惡病質小鼠模型中���,揭示了癌癥誘導的WAT功能障礙���。這項研究旨在鑒定源自惡病質誘導腫瘤的新型細胞外囊泡蛋白,闡明所涉及的潛在機制���,并探索其臨床應用的潛力���。
研究進展
GRP75對脂肪細胞褐變至關重要
GRP75是一種應激誘導的分子伴侶,屬于HSP70家族���。傳統(tǒng)上���,它作為N端信號肽定位于線粒體中,并調節(jié)蛋白質的質量控制���,包括折疊���、組裝和輸出錯誤折疊的蛋白質以進行降解���。GRP75在腫瘤組織中的過表達,通常與惡性進展呈正相關���。GRP75與血管周圍脂肪組織中的產熱脂肪細胞密切相關���,表明GRP75在腫瘤誘導的脂肪細胞褐變中的關鍵作用。
GRP75在63個ESCC組織樣本中的表達���,明顯高于相應的相鄰正常組織樣本���。GRP75表達與TNM分期之間,具有很強的相關性���。GRP75過表達與ESCC患者的不良生存率密切相關���。GRP75在其他已知的誘導惡病質的癌細胞分泌的EV中表達增強���,包括C26(小鼠結腸癌)���、HepG2(人肝細胞癌)和LLC細胞���,表明GRP75的上調與泛癌惡病質有關。
GRP75對脂肪細胞褐變至關重要���。
GRP75抑制劑在體外和體內減輕脂肪細胞褐變
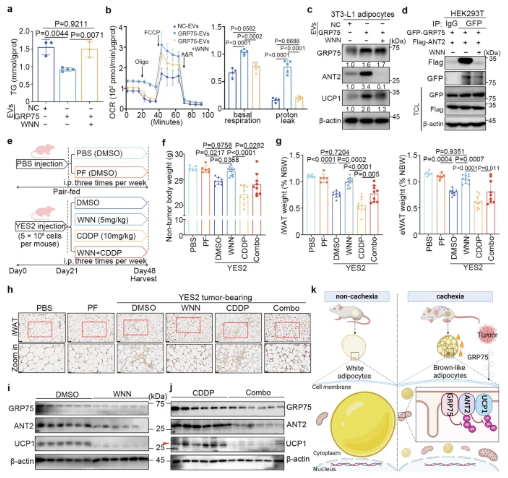
GRP75抑制劑withanone(WNN)治療阻礙了細胞內TG的降低���,以及基底和質子泄漏OCR的增加。WNN處理阻止了脂肪細胞中UCP1表達的上調���。WNN有效靶向GRP75和ANT2之間的相互作用���。這些結果表明,WNN在體外抵消GRP75過表達誘導的脂肪細胞褐變���。
WNN處理的小鼠顯示出NBW的顯著增加���,而DMSO處理的組顯示惡病質。WNN基本上抑制了YES2荷瘤小鼠的WAT萎縮和骨骼肌萎縮���。WNN治療阻止了荷瘤小鼠iWAT中脂肪細胞大小的減小���,表明WNN的抗惡病質活性���。此外,WNN處理的小鼠表現出對腫瘤生長的顯著抑制���,與CDDP處理的小鼠相當���。WNN治療有效改善了WAT褐變和隨后的惡病質狀態(tài)。這些發(fā)現表明���,WNN在體內發(fā)揮顯著的抗惡病質作用���,并抑制ESCC生長。
WNN與CDDP的組合���,大大減輕了CDDP誘導的NBW和WAT���,以及骨骼肌損失。WNN處理不會對小鼠的主要器官造成全身毒性���。這些數據表明,WNN改善順鉑誘導的脂肪褐變,而不會引起可檢測的毒性���。
GRP75抑制劑在體外和體內減輕脂肪細胞褐變���。
研究結論
脂肪組織內容和功能的改變在早期惡病質的發(fā)展中起著關鍵作用,強調了白色脂肪組織重塑在癌癥惡病質發(fā)生和進展中的重要性���。研究數據闡明了腫瘤來源的GRP75與脂肪細胞之間的通訊���,以及GRP75促進ANT2-UCP1復合物形成,以直接引發(fā)脂肪細胞褐變的分子機制���。這些結果擴展了科學界對導致惡病質發(fā)展的過程的理解���,并支持靶向腫瘤來源的GRP75作為早期癌癥惡病質干預的有前途的治療選擇。
聲明:本文版權歸原作者所有���,轉載文章僅為傳播更多信息���,如作者信息標記有誤,或侵犯您的版權���,請聯(lián)系我們���,我們將在及時修改或刪除內容���,聯(lián)系郵箱:marketing@360worldcare.com