北京大學趙穎團隊揭示“癌王”胰腺癌潛在治療策略
2月27日��,北京大學趙穎團隊在期刊《Cell Reports》上在線發(fā)表題為“UDP-glucose dehydrogenase supports autophagy-deficient PDAC growth via increasing hyaluronic acid biosynthesis”的研究論文����,在這項研究中����,研究人員發(fā)現UGDH在PDAC細胞中被自噬途徑降解。此外����,在自噬缺陷的細胞中��,積累的UGDH通過在營養(yǎng)匱乏狀態(tài)下合成HA來支持腫瘤細胞的增殖����。抑制UGDH可以減少在葡萄糖/谷氨酰胺缺乏條件下自噬缺陷細胞的生長,這可能為治療PDAC提供了潛在前景。
研究背景
癌細胞通常生長在營養(yǎng)貧乏和復雜的微環(huán)境中�����。為了在這種營養(yǎng)貧乏的環(huán)境中生存和增殖�����,癌細胞改變代謝途徑以維持其穩(wěn)態(tài)��。其中一種途徑是自噬�����,這是一種進化保守的蛋白降解過程�����,在這個過程中��,細胞內成分被包裹在自噬體內�����,然后被輸送到溶酶體進行消化�����。盡管自噬提供了重要的內部營養(yǎng)來源,但自噬缺陷的腫瘤細胞可以通過積累自噬底物或重新連接腫瘤的代謝來存活����。
例如,自噬缺陷細胞無法消除螯合體1(p62)與幾種實體瘤的腫瘤發(fā)生直接相關�����。在谷氨酰胺缺乏情況下�����,自噬缺陷的腫瘤細胞利用細胞外氨基酸產生能量并存活��。更重要的是����,氯喹(CHQ)治療對PDAC腫瘤生長僅有適度抑制作用。在臨床試驗中����,自噬抑制未能改善PDAC患者的生存率�����。因此,自噬缺陷PDAC細胞在限制性營養(yǎng)條件下的生長策略需要進一步研究��。
UDP-葡萄糖脫氫酶(UGDH)是一種獨特的酶����,能夠將UDP-葡萄糖轉化為UDP-葡萄糖醛酸(UDP-GlcUA),這是合成透明質酸(HA)的前體����。一些研究報道UGDH上調并與癌細胞的增殖、遷移和轉移有關����。與正常胰腺相比,UGDH蛋白水平在小鼠和人類PDAC中顯著提高�����。作為UGDH的下游產物��,透明質酸在PDAC基質中持續(xù)升高�����,并在PDAC中發(fā)揮促腫瘤功能。PDAC將透明質酸代謝為N-乙酰氨基葡萄糖��,以補充己糖胺生物合成途徑以支持生長��。此外����,透明質酸結合其受體CD44或CD168,通過激活PI3K/AKT和ERK信號通路刺激腫瘤生長��。
研究發(fā)現
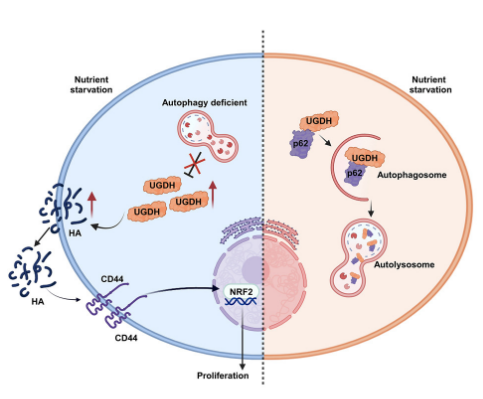
研究數據顯示��,在PDAC中的營養(yǎng)匱乏導致UDP葡萄糖脫氫酶(UGDH)降解����,這依賴于自噬貨物受體螯合體1(p62)。此外��,研究人員證明積累的UGDH通過在能量匱乏時促進透明質酸(HA)合成��,對自噬缺陷的PDAC細胞增殖至關重要����。通過使用PDAC的原位小鼠模型,研究人員發(fā)現通過靶向UGDH抑制HA合成可以減輕腫瘤重量����。因此,聯合抑制HA和自噬可能是一種吸引人的PDAC治療策略��。
研究結論
綜上所述��,在這項研究中����,研究人員發(fā)現UGDH在PDAC細胞中被自噬途徑降解。此外����,在自噬缺陷的細胞中,積累的UGDH通過在營養(yǎng)匱乏狀態(tài)下合成HA來支持腫瘤細胞的增殖�����。抑制UGDH可以減少在葡萄糖/谷氨酰胺缺乏條件下自噬缺陷細胞的生長����,這可能為治療PDAC提供了潛在前景。
聲明:本文版權歸原作者所有�����,轉載文章僅為傳播更多信息,如作者信息標記有誤����,或侵犯您的版權,請聯系我們��,我們將在及時修改或刪除內容����,聯系郵箱:marketing@360worldcare.com