NEJM:開啟醫(yī)學新時代:一個體內CRISPR基因編輯臨床試驗結果公布,安全有效
2012年8月17日���,詹妮弗·杜德娜(Jennifer Doudna)和?��,敿~埃爾·卡彭蒂耶(Emmanulle Charpentier)合作,在 Science 雜志發(fā)表了基因編輯史上的里程碑論文���,成功解析了CRISPR/Cas9基因編輯的工作原理���。她們因這項成就榮獲2020年諾貝爾化學獎。
以CRISPR/Cas9為代表的基因編輯技術���,大大加速了基因治療的快速發(fā)展���,為許多原本無藥可醫(yī)的遺傳疾病帶來了巨大的希望���。
2021年6月26日���,國際醫(yī)學期刊《新英格蘭醫(yī)學期刊》NEJM 發(fā)表了題為:CRISPR-Cas9 In Vivo Gene Editing for Transthyretin Amyloidosis 的臨床實驗論文���。
諾獎得主詹妮弗·杜德娜(Jennifer Doudna)創(chuàng)立的 Intellia Therapeutics 和再生元合作開發(fā)的治療轉甲狀腺素蛋白淀粉樣變性(ATTR)的CRISPR基因編輯療法NTLA-2001,在6名患者的臨床試驗中安全有效���。
據(jù)悉���,這也是一個公布的體內CRISPR基因編輯療法的臨床試驗結果。
轉甲狀腺素蛋白淀粉樣變性(ATTR)���,是一種危及生命的嚴重罕見遺傳疾病���,據(jù)估計,全球大約有5萬名患者���,該疾病的特征是錯誤折疊的轉甲狀腺素蛋白(TTR)蛋白在組織中逐漸積累���,主要是神經和心臟。
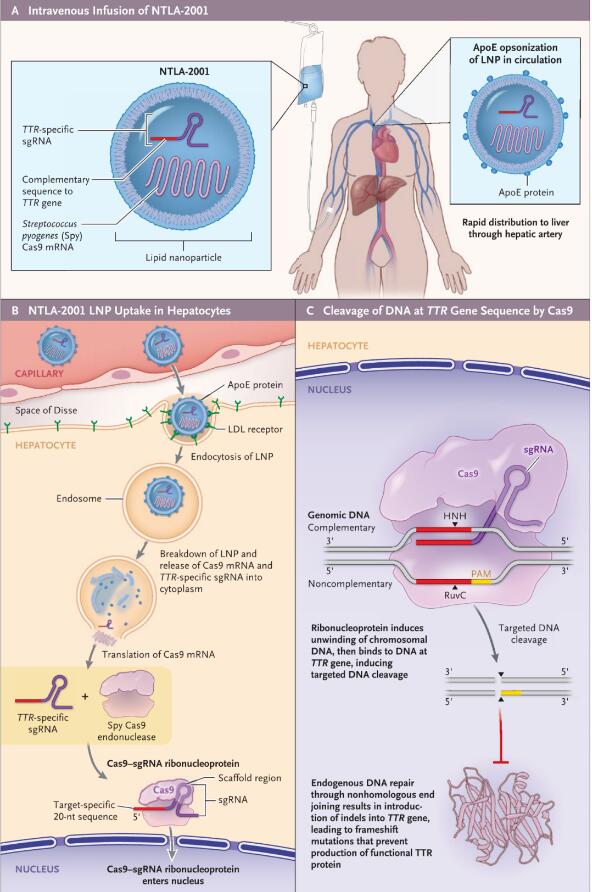
該研究使用的 NTLA-2001 療法���,是一種體內基因編輯治療���,通過脂質納米顆粒(LNP)遞送載體���,將攜帶靶向致病基因TTR基因的sgRNA和優(yōu)化的spCas9蛋白的mRNA序列,遞送至肝臟���。
臨床數(shù)據(jù)顯示���,在這6名接受治療的患者中,3名患者接受0.1mg/kg劑量���,3例患者接受0.3mg/kg劑量���。接受治療28天后,兩種不同劑量的患者血漿種TTR蛋白水平分別平均下降52%和87%���。且未觀察到嚴重不良反應���。
這是有史以來第 一個臨床數(shù)據(jù),證明可以精確地在體內進行CRISPR基因編輯,通過單次靜脈輸注CRISPR系統(tǒng)來治療遺傳疾病���。
Intellia Therapeutics 的 CEO John Leonard 表示,這項臨床試驗結果表明���,NTLA-2001 可能通過單次注射阻止轉甲狀腺素蛋白淀粉樣變性(ATTR)疾病的發(fā)展以及逆轉其破壞性并發(fā)癥���。該臨床試驗還解決了CRISPR向肝臟遞送的難題,為其他遺傳疾病的治療打開了大門���,他還表示���,將迅速推進該療法,同時擴大現(xiàn)有研發(fā)管線���。
Intellia 現(xiàn)在的研發(fā)管線
體內基因編輯療法
體外基因編輯療法
實際上���,一個開展體內CRISPR基因治療的是張鋒創(chuàng)立的 Editas Medicine,2020年3月4日���,艾爾建和 Editas Medicine 聯(lián)合宣布:CRISPR療法AGN-151587(EDIT-101)治療先天性黑蒙癥10型(LCA10)的I/II期臨床試驗���,已完成首例患者給藥���。
該臨床試驗使用的是腺相關病毒(AAV)將CRISPR基因編輯系統(tǒng)通過注射遞送到眼睛。這是全球一個體內CRISPR基因編輯臨床試驗���,也是全球首例CRISPR基因編輯的在體給藥���,據(jù)悉,該臨床試驗結果將于今年9月份公布���。
而在2020年12月5日���,《新英格蘭醫(yī)學期刊》NEJM 發(fā)表了 CRISPR Therapeutics 和 Vertex Pharmaceuticals 聯(lián)合開發(fā)的利用CRISPR/Cas9基因編輯技術治療β-地中海貧血癥和鐮狀細胞病的臨床試驗。
證實了體外CRISPR基因編輯技術在治療這兩種遺傳疾病上的安全性和有效性���。
這項體內CRISPR基因編輯療法臨床試驗結果���,大大擴展了CRISPR基因編輯療法的應用范圍,能夠直接通過注射在體內進行高效基因編輯���,為許多遺傳疾病的治療開辟了新的途徑���,可以說是開啟了醫(yī)學新時代���。
原始出處:
Julian D. Gillmore, et al. CRISPR-Cas9 In Vivo Gene Editing for Transthyretin Amyloidosis. NEJM���, June 26, 2021. DOI: 10.1056/NEJMoa2107454
聲明:本文版權歸原作者所有���,轉載文章僅為傳播更多信息���,如作者信息標記有誤,或侵犯您的版權���,請聯(lián)系我們���,我們將在及時修改或刪除內容,聯(lián)系郵箱:marketing@360worldcare.com